
LA RADIOATTIVITA'
LA RADIOATTIVITA' NATURALE
Esatto, la scoperta della radioattività naturale da parte di Henri Becquerel nel 1896 è stato un evento fondamentale nella storia della fisica.Becquerel osservò che alcuni sali di uranio erano in grado di emettere una radiazione penetrante simile ai raggi X scoperti da Wilhelm Roentgen un anno prima.Successivamente si scoprì che questa radiazione era dovuta alla presenza di atomi instabili che si trasformavano nel tempo, formando nuovi atomi.Questi atomi instabili sono noti come elementi radioattivi. L'emissione di particelle da parte di questi atomi instabili avviene secondo una legge chiamata legge del decadimento radioattivo.La legge del decadimento radioattivo descrive il decadimento esponenziale di un campione radioattivo nel tempo.La quantità di nuclei instabili rimanenti nel tempo t può essere descritta dall'equazione N(t) = N₀ * e^(-λt), dove N(t) è il numero di nuclei instabili al tempo t, N₀ è il numero iniziale di nuclei instabili, λ è la costante di decadimento specifica per l'elemento radioattivo considerato, e e è la base del logaritmo naturale.Da questa legge deriva la definizione del tempo di dimezzamento (T(⅟₂)), che rappresenta il tempo necessario affinché il numero di nuclei instabili si dimezzi.Il tempo di dimezzamento è calcolato come T(⅟₂) = (ln 2)/λ, dove ln rappresenta il logaritmo naturale.Il tempo di dimezzamento varia notevolmente da un elemento radioattivo all'altro.Ci sono isotopi radioattivi con tempi di dimezzamento dell'ordine dei secondi, mentre altri possono avere tempi di dimezzamento paragonabili all'età della Terra.Questa variabilità nei tempi di dimezzamento è determinata dalle proprietà specifiche di ogni isotopo radioattivo.La radioattività naturale e lo studio del decadimento radioattivo hanno avuto un impatto significativo nella fisica nucleare, nella datazione di materiali geologici e archeologici, nonché in molte applicazioni tecnologiche.
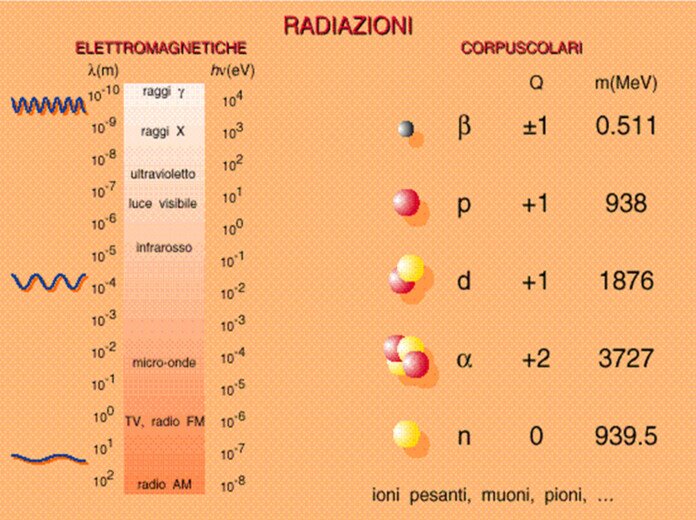
Spettro eletromagnetico delle radiazioni
Esistono diversi tipi decadimenti radioattivi: i principali sono il decadimento alfa e il decadimento beta, tra cui il decadimento alfa e il decadimento beta.Nel decadimento alfa, un nucleo instabile emette una particella alfa, che è costituita da due protoni e due neutroni, equivalenti ad un nucleo di elio (He).Questo tipo di decadimento provoca una diminuzione di due unità nel numero atomico Z e di quattro unità nel numero di massa A dell'atomo.Di conseguenza, l'atomo figlio che si forma dopo il decadimento avrà due posizioni in meno nella tavola periodica rispetto all'atomo padre.Ad esempio, l'uranio-238 può decadere emettendo una particella alfa e trasformandosi in torio-234.Il decadimento beta si verifica in due forme: decadimento beta meno e decadimento beta più.Nel decadimento beta meno, un neutrone del nucleo instabile si trasforma in un protone, emettendo un elettrone (chiamato elettrone beta) e un antineutrino.Con questo tipo di decadimento, il numero atomico dell'atomo aumenta di una unità, poiché un neutrone si trasforma in un protone, e l'atomo si trasforma nell'elemento successivo nella tavola periodica.Tuttavia, il numero di massa rimane lo stesso.Nel decadimento beta più, un protone si trasforma in un neutrone, emettendo un positrone (un elettrone di carica positiva) e un neutrino elettronico.Con questo tipo di decadimento, il numero atomico dell'atomo diminuisce di una unità, poiché un protone si trasforma in un neutrone, e l'atomo si trasforma nell'elemento precedente nella tavola periodica.Anche in questo caso, il numero di massa rimane invariato.Questi diversi tipi di decadimenti radioattivi sono importanti per la comprensione della stabilità nucleare e delle trasformazioni degli atomi instabili in altri elementi.
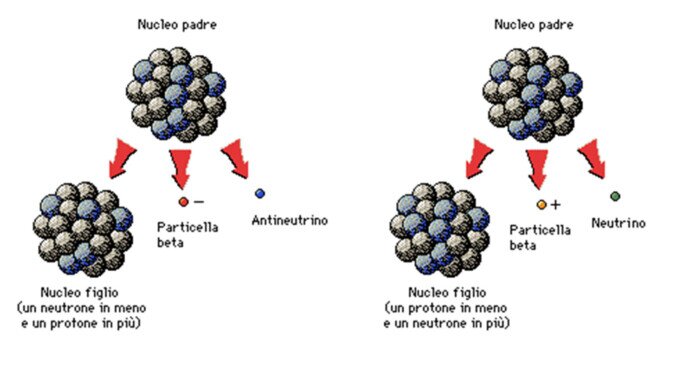
Decadimenti beta
Pericolosità delle particelle alfa a, beta b e gamma g.
Le particelle alfa (α) sono costituite da nuclei di elio e sono relativamente grandi e pesanti. A causa delle loro dimensioni e della loro carica positiva, le particelle alfa hanno una bassa capacità di penetrazione e vengono facilmente fermate da un foglio di carta o pochi centimetri di aria. Tuttavia, se vengono inalate, ingerite o penetrano nella pelle attraverso una ferita, possono causare danni significativi ai tessuti biologici circostanti.Le particelle beta (β) sono costituite da elettroni (β-) o positroni (β+). Sono più piccole e leggere rispetto alle particelle alfa e hanno una maggiore capacità di penetrazione. Possono attraversare alcuni centimetri di aria o alcuni millimetri di tessuti corporei. Le particelle beta possono causare danni ai tessuti biologici, specialmente se sono assorbite internamente nel corpo attraverso l'inalazione, l'ingestione o l'assorbimento cutaneo.Le radiazioni gamma (γ) sono costituite da fotoni ad alta energia e sono estremamente penetranti. Possono attraversare facilmente il corpo umano e richiedono schermature di materiali densi, come il piombo o il cemento, per essere attenuate. Le radiazioni gamma possono causare danni ai tessuti biologici, in particolare al DNA, e sono considerate le più pericolose in termini di rischio di radiazione.
PARTICELLE ALFA (a)
Per la natura di scarsa penetrazione in sostanze dense, le particelle alfa emesse da radioelementi, anche quelle di più alta energia, riescono al massimo a penetrare lo strato morto della pelle del corpo umano e non raggiungono il tessuto vivente per cui non si può riscontrare un rischio di danno biologico.Tuttavia, per la contaminazione interna, essa rappresenta un pericolo più grave. Come è già stato indicato, le particelle alfa hanno una scarsa penetrazione nelle sostanze dense e si concentrano principalmente sullo strato superficiale. Quando queste particelle si depositano in un organo interno, tutta la loro energia viene assorbita in quella zona limitata e non si distribuisce su una massa più grande di tessuto. Questo può causare danni significativi all'organo colpito. Pertanto, la radiazione alfa può essere pericolosa quando avviene una contaminazione interna, poiché l'energia concentrata può danneggiare gravemente l'organo in cui si deposita.
PARTICELLE BETA (b)
Le particelle beta (b) consistono in elettroni o positroni emessi dai nuclei instabili degli atomi radioattivi.Possono essere emessi sia elettroni negativi che positroni, differenziandosi solo per il segno della carica, ma con la stessa massa a riposo.A differenza delle particelle alfa (a), le particelle beta (b) non vengono emesse con un'energia fissa e ben determinata, ma variano in uno spettro continuo fino al loro valore massimo di energia, che è caratteristico per ogni radioisotopo.Quando le particelle beta interagiscono con la materia, perdono gradualmente la loro energia e riducono il loro movimento cinetico.Ciò avviene principalmente attraverso due processi: collisione con gli elettroni orbitali, che porta a una perdita di energia che si traduce in eccitazione e ionizzazione, e interazione con i nuclei, che può portare all'emissione di raggi X (questo processo avviene principalmente quando le particelle beta hanno energie elevate).A causa della loro massa molto più piccola rispetto alle particelle alfa, le particelle beta hanno interazioni meno frequenti con la materia e quindi hanno una minore ionizzazione specifica rispetto alle particelle alfa, a parità di condizioni.Nei gas, ad esempio nell'aria, i valori di ionizzazione per gli elettroni (particelle beta) variano da 60 a 7.000 coppie ioni/cm, mentre per le particelle alfa corrispondono a valori da 10.000 a 70.000 coppie ioni/cm.Il potere frenante degli elettroni diminuisce quando aumenta il numero atomico Z della sostanza assorbente, poiché le sostanze con Z elevato hanno una minore densità di elettroni, che sono più strettamente legati al nucleo.Tuttavia, all'aumentare di Z, aumenta anche la diffusione multipla degli elettroni, il che comporta un aumento del loro percorso effettivo nella sostanza.Pertanto, la densità di una sostanza offre un'indicazione della sua capacità di arrestare le particelle beta, anche se in generale l'assorbimento degli elettroni è spesso espresso in mg/cm2 ed è approssimativamente indipendente dal tipo di composto organico assorbente.L'assorbimento delle particelle beta da parte della materia segue una legge precisa di decadimento esponenziale caratterizzata dal coefficiente di assorbimento della massa m.Le particelle beta possono rappresentare un rischio per danni biologici sia nell'irradiazione esterna che nella contaminazione interna.
PARTICELLE GAMMA (g)
Le radiazioni gamma (g) sono simili alle radiazioni X e consistono in fotoni, che sono particelle di luce o radiazione elettromagnetica.A differenza delle particelle alfa (a) e beta (b), le radiazioni gamma sono neutre e si propagano alla velocità della luce (c = 3 x 10^8 m/s).Sono generate nei processi di rilassamento del nucleo atomico.Le radiazioni gamma sono estremamente penetranti e possono attraversare sia l'aria che il tessuto organico con scarsa assorbimento.A causa della loro elevata capacità di penetrazione, le radiazioni gamma possono rappresentare un rischio significativo per il danno biologico e genetico.Durante l'irraggiamento, i fotoni gamma presentano un alto grado di pericolosità per due motivi:
- Penetrazione: I fotoni gamma possono penetrare per distanze considerevoli dalla sorgente senza essere significativamente assorbiti. Ciò richiede schermature molto più consistenti rispetto alle particelle alfa (a) e beta (b) per proteggere dalle radiazioni gamma.
- Esposizione dei tessuti radiosensibili: Poiché i fotoni gamma attraversano la materia facilmente, i tessuti più radiosensibili del corpo umano possono essere esposti ai campi di radiazione esterna. Ciò aumenta il rischio di danni biologici, che non rimangono limitati solo ai tessuti superficiali meno importanti.
È importante adottare adeguate misure di protezione, come l'utilizzo di schermature adeguate, per ridurre l'esposizione ai raggi gamma e minimizzare il rischio di danni biologici.


 Italiano
Italiano English
English Español
Español Français
Français Deutsch
Deutsch العربية
العربية